La Plateforme Imathéra
Les projets de recherche d’IMATHERA s’articulent autour de 4 axes majeurs : la cancérologie, la fibrose pulmonaire, les atteintes cardiovasculaires et la méthodologie en imagerie préclinique.
Ensemble, dépassons le cancer.
Plateforme Imathera
L’imagerie moléculaire est devenue depuis de nombreuses années un outil crucial pour la détection et la prise en charge des cancers. Depuis 2011, le service de Médecine Nucléaire du Centre Georges-François Leclerc s’implique dans la recherche translationnelle en imagerie en accueillant la plateforme IMATHERA qui permet une approche complète de la pharmaco-imagerie et la thérapie par les radiations dans un cadre exclusivement dédié.
Grâce à sa localisation stratégique au sein du campus universitaire dijonnais et son appartenance au GIE Pharm’image®, le CGFL travaille avec de nombreux partenaires locaux hautement spécialisés dans des domaines complémentaires allant de la conception de molécules pour la radioimagerie (ICMUB, CheMatech) au traitement d’images réalisées chez le patient (CGFL, CHU Dijon) en passant par les étapes de validations précliniques (Oncodesign, IMATHERA) ce qui constitue un champ d’expertise local unique. La proximité avec des centres de recherche éminents (INSERM, UB, CNRS) et des cliniciens permet à IMATHERA de s’inscrire dans une démarche de recherche translationnelle dédiée aux patients.
La plateforme IMAHTERA est certifiées selon la norme Organisation internationale de normalisation ISO 9001 depuis 2024, attestant de la mise en œuvre d’un système de management de la qualité structuré, orienté vers la satisfaction des patients et des partenaires, l’amélioration continue des processus et la maîtrise des risques de ses activités d’Imagerie préclinique et de radiobiologie.

Nos principaux partenaires


Nos moyens
La plateforme d’imagerie préclinique, au sein du service de médecine nucléaire dirigé par le Pr Alexandre Cochet (PU-PH), dispose d’un laboratoire de 575 m² totalement dédié à l’imagerie préclinique est accrédité par l’Autorité de Sureté Nucléaire (ASN) et la Direction Départementale de la Protection des Populations (DDPP). Son personnel hautement spécialisé inclut une équipe pluridisciplinaire dirigée par le Dr Bertrand Collin, radiopharmacien enseignant-chercheur responsable de la plateforme, le Dr Alexandra Oudot, responsable adjointe, le Dr Pierre-Simon Bellaye, responsable de la recherche, le Dr Alexandre Dias et le Dr Romain Douhard, chercheurs et Alex Helbling, directeur d’étude. L’équipe compte également un radiophysicien (Dr Jean-Marc Vrigneaud), deux personne compétente en radioprotection (Lydie Houot et Mickaël Pichon) et un chercheur en imagerie TEP/IRM (Dr Alan Courteau). Les travaux d’IMATHERA reposent sur une équipe technique hautement spécialisée (John Simonet et Mélanie Guillemin) et des étudiants (Romain Fontaine–Tuffery, Agnieszka Kownacka, Sarah Jedidi, Jame Frenay et Camille Petitot, doctorants).
Grâce aux laboratoires de radiochimie, radiomarquage et contrôle qualité, il y est possible de concevoir des sondes d’imagerie innovantes à façon en se basant sur des équipements de dernière génération. Les sondes moléculaires sont ensuite évaluées in vitro et in vivo grâce à un panel complet d’équipement permettant d’adapter la technologie de détection à la problématique biologique : caméra de scintigraphie couplée à un scanner, TEP (tomographie par émission de positons) couplée à un scanner, TEP couplée à l’IRM (imagerie de résonance magnétique) , imagerie optique, ou imagerie 2D.
Depuis 2012, IMATHERA accueille le programme Equipex des « investissements d’avenir » IMAPPI (Integrated Magnetic resonance And Positron emission tomography in Preclinical Imaging) financé par l’agence nationale pour la recherche (ANR) à hauteur de 7,3 millons € et dirigé par le Pr François Brunotte (PU-PH). Ce projet a pour objectif de développer un nouvel imageur préclinique unique en Europe, alliant la haute sensibilité de la TEP avec la haute résolution de l’IRM. Cette technologie n’est à l’heure actuelle disponible que dans très peu de sites au monde et uniquement sous forme de prototype. La PIRP bénéficie également de financements émanant d’institutions publiques (ANR, région Bourgogne Franche-comté…) et d’associations (ligue contre le cancer, fondation d’avenir, ARC, Fonds de Recherche en Santé Respiratoire…) pour mener à bien ses projets de recherche.
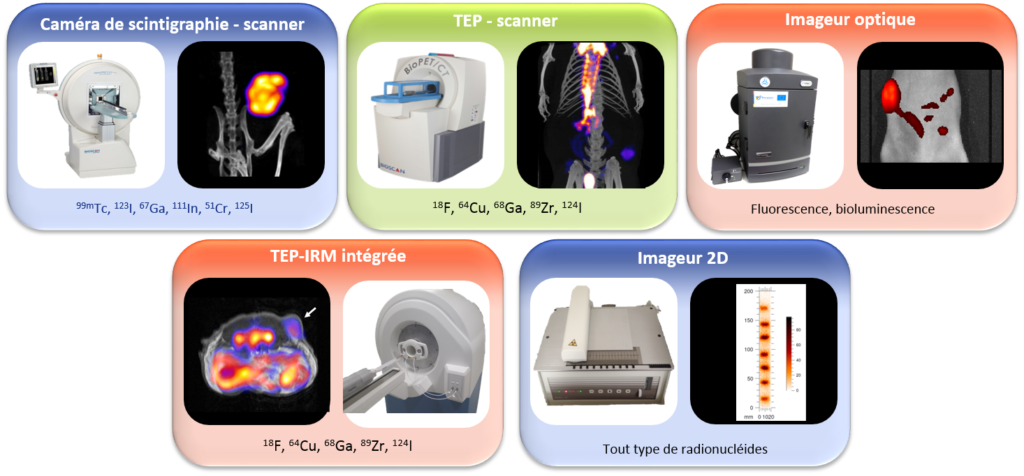
Dans chaque étude menée sur la plateforme, une attention particulière est apportée pour se rapprocher au maximum des conditions cliniques rencontrées chez les patients en adaptant au mieux au vivant les sondes d’imagerie développées. Pour ce faire, des modèles se rapprochant le plus possible de la pathologie humaine sont employés en utilisant les mêmes modalités d’imagerie que dans le service clinique de médecine nucléaire.
Nos principaux projets
CANCÉROLOGIE
RADIOTHERAPIE INTERNE VECTORISÉE – Le projet COMETE
Le projet COMETE (moleCular radiOtherapy for METastatic Colorectal and gastric cancErs) répond à l’appel à projet régional FEDER-FSE+. Il porte sur le développement d’un portefeuille de molécules de de radiothérapie interne vectorisée (RIV) pour le diagnostic et le traitement de cancers digestifs avancés. Le projet a pour but de développer deux candidats RIV jusqu’aux études de dosimétrie préclinique, juste avant un passage en évaluation clinique. Le projet COMETE est porté par un consortium constitué de la société Oncodesign Precision Medicine (OPM), de l’Institut de Chimie Moléculaire de l’Université de Bourgogne (ICMUB, UMR CNRS 6302) et du CGFL, tous basés à Dijon.

La Radiothérapie Interne Vectorisée (RIV) est une innovation thérapeutique de rupture pour le traitement de certains cancers métastatiques. Elle consiste en l’administration aux patients de petites molécules porteuses d’un atome radioactif, qui vont reconnaitre et se fixer sur une « cible » exprimée ou surexprimée par les cellules tumorales. La radioactivité ainsi délivrée directement sur les cellules tumorales va provoquer des dommages sur leur ADN et ainsi stopper la progression de la maladie. Ces traitements sont administrés sous la responsabilité des médecins nucléaires, en étroite collaboration avec les oncologues médicaux.
LA RIV EN 4 ACTES :
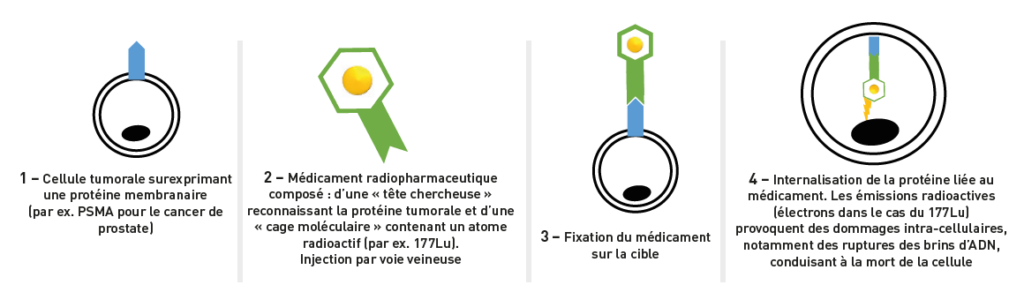
L’autre avantage majeur de la RIV est la possibilité de combiner ces traitements avec des outils diagnostiques « compagnons » : la même molécule qui cible la tumeur peut être utilisée pour obtenir des images en Tomographie par Emission de Positons (TEP), permettant de vérifier que la cible est bien exprimée par les tumeurs. On parle d’approche « théranostique » (« théra » étant la contraction de thérapie et « nostique » la contraction de diagnostique). Ces images réalisées avant RIV vont permettre de prédire l’efficacité du traitement, et donc de ne le proposer qu’aux patients susceptibles d’en bénéficier. Cette stratégie théranostique, qui permet également le suivi d’efficacité des traitements RIV, s’inscrit donc dans une démarche de médecine personnalisée.
Les cancers digestifs représentent plus de 20% des cancers en France, parmi lesquels les cancers colorectaux, gastriques et pancréatiques correspondent respectivement à 61%, 12% et 8%. Le cancer colorectal est le 2ème cancer le plus diagnostiqué chez la femme et le 3ème chez l’homme. La chirurgie est la base du traitement des pathologies locales et loco-régionales. Cependant, près de 50% des patients avec un cancer colorectal vont développer des métastases, ce qui contribue à un fort taux de mortalité face à l’échec des thérapies actuelles. L’essor de nouvelles stratégies thérapeutiques pour le cancer colorectal, combinant la chirurgie, la radiothérapie et la chimiothérapie, n’a pas permis une amélioration significative de la survie à 5 ans des patients métastatiques, qui reste inférieure à 10%.
Le cancer gastrique est le 5ème cancer le plus couramment diagnostiqué et la 3ème cause de mortalité dans le monde. Le pronostic des cancers gastriques est lié au stade de la maladie au moment du diagnostic. L’offre thérapeutique pour les cancers gastriques à un stade avancé, caractérisés par l’apparition de métastases, est très limitée. Notamment, la présence de métastases cérébrales aggrave le pronostic et la médiane de survie moyenne est comprise entre 1,3 et 2,4 mois.
Le cancer pancréatique est le 6ème cancer le plus couramment diagnostiqué en France et la 4ème cause de mortalité chez les femmes et la 5ème chez les hommes. La survie à 5 ans des patients atteints de cancer pancréatique est inférieure à 4%, c’est donc un cancer avec un pronostic très mauvais.
Dans ce projet, nous proposons de développer des traitements par radiothérapie interne vectorisée (RIV), permettant de répondre à ce besoin clinique non satisfait et d’augmenter la survie des patients présentant des cancers digestifs métastatiques.
Le projet COMETE s’articule autour de 4 objectifs scientifiques principaux :
- L’identification et la validation de cibles tumorales dans les cancers digestifs métastatiques, via des approches d’intelligence artificielle et des plateformes technologiques innovantes pour la production de vecteurs biologiques très spécifiques.
- Le développement de nouvelles molécules de RIV pour traiter les cancers digestifs métastatiques, de leur conception et leur optimisation à la sélection de la meilleure molécule en vue de son développement chez l’Homme en phase précoce.
- L’évaluation de l’efficacité anti-tumorale et de la toxicité des molécules de RIV sur des modèles précliniques de cancers colorectaux et gastriques métastatiques.
- Le développement d’agents d’imagerie “compagnons” de la RIV, pour permettre la personnalisation de la prise en charge thérapeutique (sélection des patients répondeurs, optimisation de la dose, suivi de l’efficacité).
Tumeur solide – Cancer du sein TRIPLE Negatif
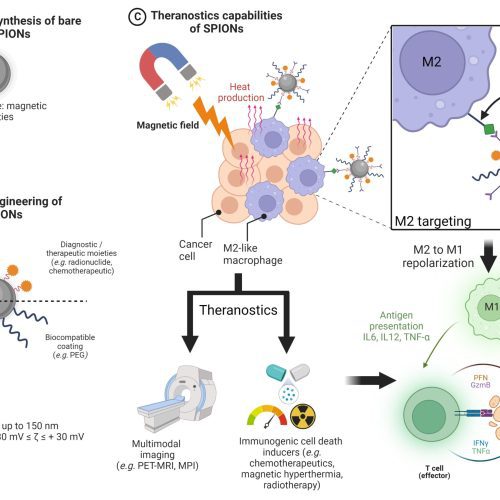
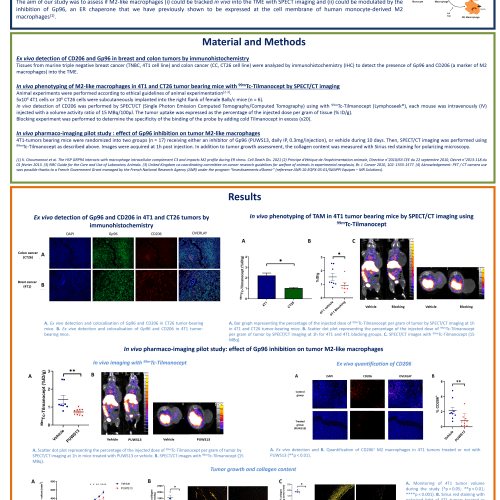
Parmi les différents types de cancers du sein, le cancer du sein dit triple négatif est constitué de cellules tumorales n’exprimant pas les récepteurs ciblés par la plupart des thérapies innovantes aujourd’hui disponibles pour les autres types de cancer du sein. Ce cancer est particulièrement agressif et associé à une grande mortalité avec une survie à 5 ans inférieure à 25%. Son traitement reste aujourd’hui un véritable défi car aucune thérapie ciblée ne peut être proposée. Le cancer du sein triple négatif est caractérisé par une infiltration de cellules immunosuppressives qui, en supprimant les réponses immunitaires antitumorales, favorisent la progression des tumeurs et le développement de métastases. Notre projet vise donc d’une part à développer de nouveaux médicaments visant ces cellules immunosuppressives et, d’autre part, à valider des marqueurs de suivi thérapeutique de tels traitements.
Notre équipe travaille actuellement en collaboration avec l’équipe INSERM HSP-pathies dirigée par le Dr Carmen Garrido sur une protéine de stress : Gp96, dont la présence augmentée dans certaines tumeurs est associée à un mauvais pronostic. Nous avons montré que Gp96 était présente à la membrane d’un type de macrophages immunosuppresseurs : les macrophages M2, dont l’expression est corrélée à un mauvais pronostic. Nous avons pu imager in vivo par imagerie SPECT ces macrophages immunosuppresseurs dans nos modèles de cancer du sein triple négatif et suivre leur diminution lors de l’utilisation d’un inhibiteur de Gp96. Ainsi l’imagerie de ces macrophages immunosuppresseurs pourrait être un outil innovant en tant que marqueur potentiel pour le pronostic, la prédiction thérapeutique et/ou le suivi dans le cancer du sein triple négatif.
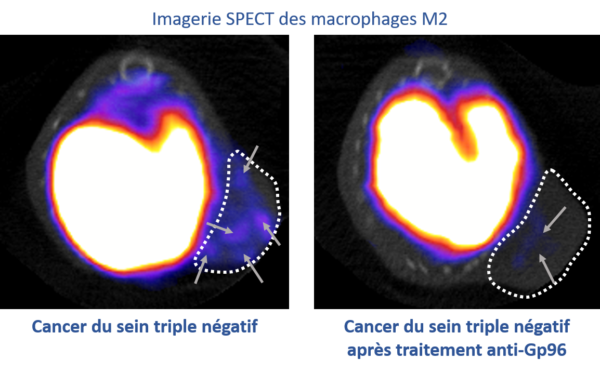
Publications associées:
- Bouchard A, Sikner H, Baverel V, Garnier AR, Monterrat M, Moreau M, Limagne E, Garrido C, Kohli E, Collin B, Bellaye PS. The GRP94 Inhibitor PU-WS13 Decreases M2-like Macrophages in Murine TNBC Tumors: A Pharmaco-Imaging Study with 99mTc-Tilmanocept SPECT. Cells. 2021 Dec 2;10(12):3393
- Chaumonnot, S. Masson, H. Sikner, A. Bouchard, V. Baverel, P. S. Bellaye, B. Collin, C. Garrido, E. Kohli, The HSP GRP94 interacts with macrophage intracellular complement C3 and impacts M2 profile during ER stress. Cell Death Dis 12, 114 (2021).
- 99mTc-Timanocept Spect Imaging As A Potential Non-Invasive Method To Quantify CD206+ Tumor-Associated M2-like Macrophages, EMIM 2021 (poster)
Tumeur solide – Cancer du sein HER2-faible
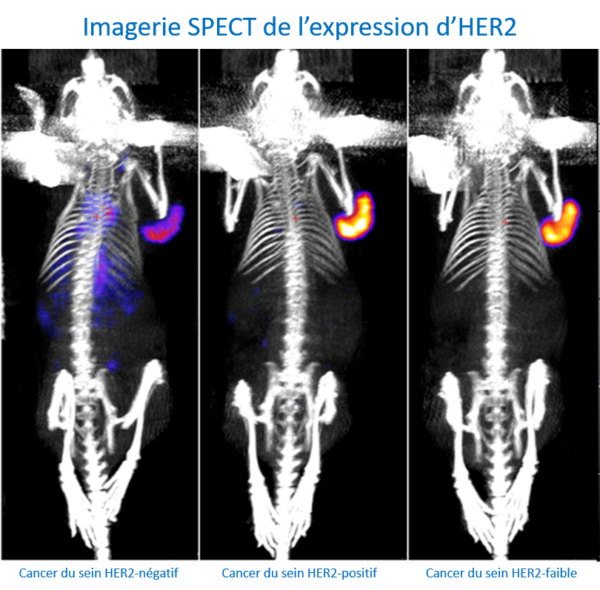
Le cancer du sein est le cancer le plus répandu dans le monde. En effet, les tumeurs mammaires chez la femme représentent à elles seules environ 11,7 % des nouveaux cas de cancer chaque année, avec plus de deux millions de femmes diagnostiquées en 2020, faisant de cette maladie un problème majeur de santé publique. Au niveau moléculaire, cette tumeur maligne est très hétérogène et peut être divisée en cinq groupes (cancer du sein de type Luminal A, Luminal B HER2 négatif, Luminal B HER2 positif, enrichi en HER2, triple négatif) en fonction de l’expression immunohistochimique des récepteurs des œstrogènes, des récepteurs de la progestérone et du récepteur 2 du facteur de croissance épidermique humain (HER2). Environ 20 % des cas de cancer du sein nouvellement diagnostiqués sont HER2-positifs et le pronostic de ce groupe s’est amélioré avec la thérapie ciblée anti-HER2 basée sur anticorps monoclonaux. Malgré ce progrès, un pourcentage élevé de patients (40-50%) présente une faible expression de HER2 (HER2-faible) auprès desquels les thérapies anti-HER2 sont peu efficaces. Cependant, des études récentes ont montré que les patients HER2-faible pourraient bénéficier de nouvelles thérapies ciblant HER2 basées sur des anticorps « armés » (Antibody drug conjugates, ADC). Cependant, des phénomènes de résistance à ces nouvelles thérapies ont été observés. De plus, la détermination précise de l’expression d’HER2 est essentielle pour identifier les patientes qui pourraient bénéficier de ces thérapies, principalement lorsque les tests de référence actuels pour la détermination de l’expression HER2-faible/HER2-négatif ont été contestés en raison de leur faible précision. Ces données nous ont conduits à émettre l’hypothèse que la production de sondes théranostiques (combinant des propriétés pour le diagnostique et la thérapie) ciblant HER2, dans un contexte de type HER2-faible, pourrait représenter une approche innovante pour surmonter les problèmes actuels et ainsi améliorer le diagnostic et la prise en charge thérapeutique de ces patientes.
Nos résultats préliminaires ont montré que l’imagerie nucléaire, grâce à une sonde spécifique d’HER2, pouvait détécter le niveau d’expression d’HER2 dans divers modèles précliniques de cancer du sein. Ces résultats ont permis à notre plateforme d’obtenir un financement ANR (EITHER2BC) de 324 000 euros sur 3 ans (2023-2026) pour développer ces sondes pour le diagnostic et la thérapies des cancers du sein HER2-low.
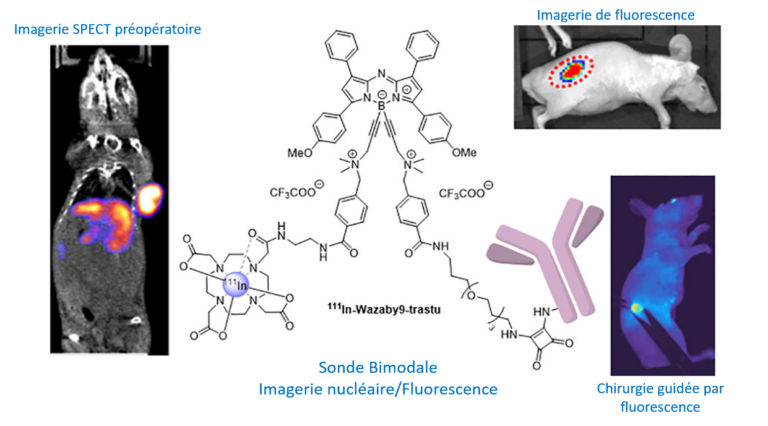
Tumeur solide – Chirurgie guidée par fluorescence
Malgré l’émergence des thérapies ciblées, la chirurgie joue toujours un rôle essentiel dans le traitement des cancers colorectal et pancréatique. Un problème majeur réside dans la difficulté de détecter et de visualiser les marges tumorales. La chirurgie guidée par fluorescence (FGS) permet aux chirurgiens une meilleure visualisation des structures anatomiques en temps réel. De plus, la FGS peut être améliorée en associant une imagerie pré-opératoire pour localiser avec précision les tumeurs. Dans ce projet, nous proposons de concevoir et d’évaluer des conjugués d’imagerie bimodale (imagerie nucléaire/fluorescence) afin d’améliorer la stadification pré-opératoire (SPECT), la détection per-opératoire des tumeurs et leur résection (FGS) mais aussi d’améliorer le suivi post-opératoire (SPECT). Nos sondes seront testées pour la FGS dans différents modèles précliniques mimant la pathologie humaine, tels que des modèles orthotopiques de cancer du côlon et du pancréas, mais aussi des modèles mimant la formation de métastases hépatiques ou de carcinomatose péritonéale. Les résultats attendus de ce projet sont, une visualisation fine des tumeurs avant la chirurgie (imagerie SPECT) et une détection plus précise par fluorescence permettant de minimiser l’étendue de la résection. Enfin, l’absence de récidive pourra être détectée en utilisant ce composé quelques semaines après la chirurgie (SPECT).
Ce projet a permis à notre plateforme de contribuer à un projet financé par l’INCA (PLBIO23-023) à hauteur de 593 460 euros sur 3 ans (2023-2026) porté par le Dr Catherine Paul (École Pratique des Hautes Études – Université PSL) et en collaboration avec l’ICMUB (Dr Goze Christine) et le CHU de Besançon (Dr Doussot Alexandre).
Publications associées:
- M. Privat , A. Massot , F. Hermetet, H. Al Sabea, C. Racoeur, N. Mabrouk , M. Cordonnier, M. Moreau, B. Collin, A. Bettaieb, F. Denat, E. Bodio, PS Bellaye, C. Goze, C. Paul. Development of an Immuno-SPECT/Fluorescent Bimodal Tracer Targeting Human or Murine PD-L1 on Preclinical Models. J Med Chem 2024.
- Privat M, Bellaye PS, Chazeau E, Racoeur C, Adumeau P, Vivier D, Bernhard C, Moreau M, Collin B, Bettaieb A, Denat F, Bodio E, Paul C, Goze C. First Comparison Study of the In Vitro and In Vivo Properties of a Randomly and Site-Specifically Conjugated SPECT/NIRF Monomolecular Multimodal Imaging Probe (MOMIP) Based on an aza-BODIPY Fluorophore. Bioconjug Chem 2023.
- M. Privat, P. S. Bellaye, R. Lescure, A. Massot, O. Baffroy, M. Moreau, C. Racoeur, G. Marcion, F. Denat, A. Bettaieb, B. Collin, E. Bodio, C. Paul, C. Goze, Development of an Easily Bioconjugatable Water-Soluble Single-Photon Emission-Computed Tomography/Optical Imaging Bimodal Imaging Probe Based on the aza-BODIPY Fluorophore. J Med Chem, (2021).
Hématologie – lymphome / myélome
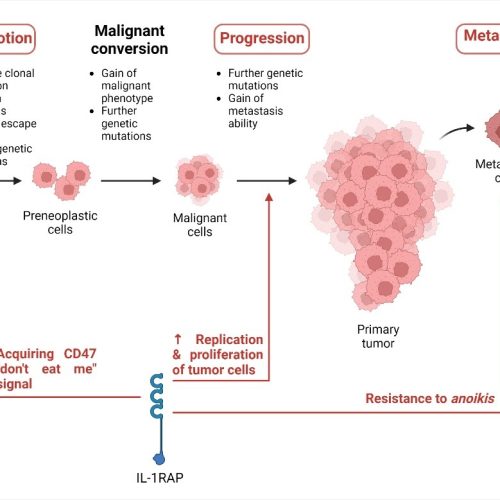
Nos projets en hématologie visent à développer de nouveaux agents d’imagerie afin de mieux détecter ces cancers et offrir des solutions facilitant le suivi des patients et les décisions thérapeutiques. Notre recherche se focalise sur 2 cibles principale: la protéine IL-1RAP, impliquée dans l’inflammation et le développement des tumeurs, est retrouvé surexprimée dans plusieurs cancers, et notamment les leucémies myéloïdes aiguës et chroniques. Et le récepteur CD38, actuellement utilisé en clinique dans le traitement des myélomes, les anticorps anti-CD38 (ex.: Daratumumab) pourraient également se montrer efficace dans certaines formes de lymphomes, comme le lymphome de Burkitt qui touche essentiellement les enfants et jeunes adultes.
Les cancers hématologiques ou “cancer du sang” touchent environ 35 000 personnes chaque année en France et concernent principalement les enfants, jeunes adultes et personnes âgées. Les leucémies, lymphomes, myélomes sont les plus fréquents. Les cancers hématologiques surviennent lors d’un dysfonctionnement de la maturation des cellules du sang : globules blancs, globules rouges et plaquettes, qui favorisent leur prolifération anormale. Les cellules du sang se développent d’abord dans la moelle osseuse, au cœur des os, avant d’être diffusées dans le sang. L’accumulation de cellules sanguines altérées freine le fonctionnement normal des autres cellules (lutte contre les infections, prévention des saignements…). Plus les altérations apparaissent tôt dans le processus de maturation, plus l’agressivité du cancer risque d’être élevée. La découverte de nouveaux biomarqueurs précoces de la progression et de l’efficacité des traitements dans ce type de pathologie est cruciale pour l’amélioration de la prise en charge des patients.
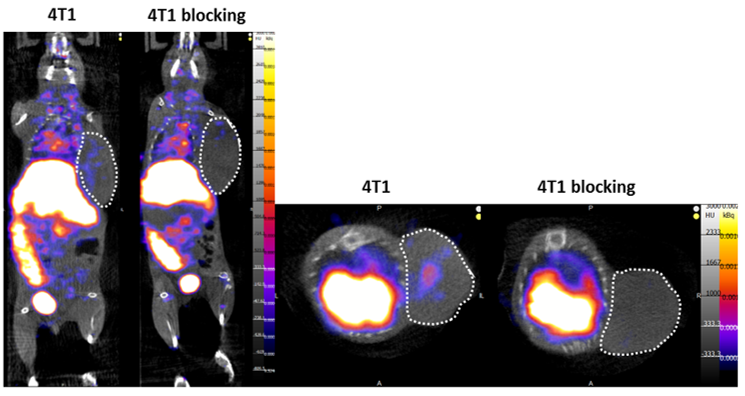
Dans ce contexte, nous travaillons en collaboration avec le Dr Christophe Ferrand (CanCell Therapeutics, Besançon) pour le développement d’un biomarqueur compagnon d’imagerie pour une nouvelle thérapie « CAR-T cells » ciblant IL-1RAP. Cette thérapie innovante est actuellement en phase d’essai clinique (CHU Besançon, CanCell Therapeutics) et un biomarqueur compagnon d’imagerie ciblant IL-1RAP pourrait permettre de mieux sélectionner les patients présentant une surexpression de cette cible et pour lesquels cette thérapie aura le plus de chance de fonctionner. Notre objectif est donc de mettre au point un compagnon de diagnostique basé sur une anticorps ciblant IL-1RAP modifié afin de le visualiser par imagerie médicale en incorporant un isotope radioactif visible par imagerie PET/CT, SPECT/CT et/ou PET/IRM. Via cette technologie, il est également possible de remplacer l’isotope radioactif d’imagerie par un autre isotope plus irradiant permettant ainsi d’obtenir un agent thérapeutique via la technique de radiothérapie interne vectorisée afin d’éliminer spécifiquement les cellules tumorales.
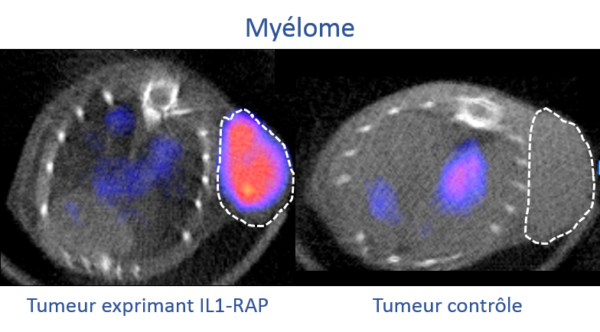
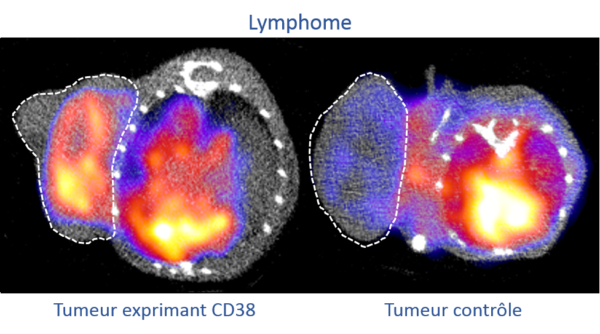
Afin de démontrer l’utilité du ciblage du récepteur CD38 dans les lymphomes, nous testons aujourd’hui des anticorps anti-CD38 dans différents modèles de lymphomes en collaboration avec le service d’hématologie du CHU de Dijon. Pour ce faire, nous modifions légèrement ces anticorps afin de pouvoir les observer via les techniques d’imagerie médicale (PET/CT, SPECT/CT, PET/IRM). Dans ce contexte, il est également possible de remplacer l’isotope radioactif d’imagerie par un autre isotope plus irradiant permettant ainsi d’obtenir un agent thérapeutique via la technique de radiothérapie interne vectorisée afin d’élimer spécifiquement les cellules tumorales.
Imagerie des thérapies cellulaires (ex: Cellules CAR-T)
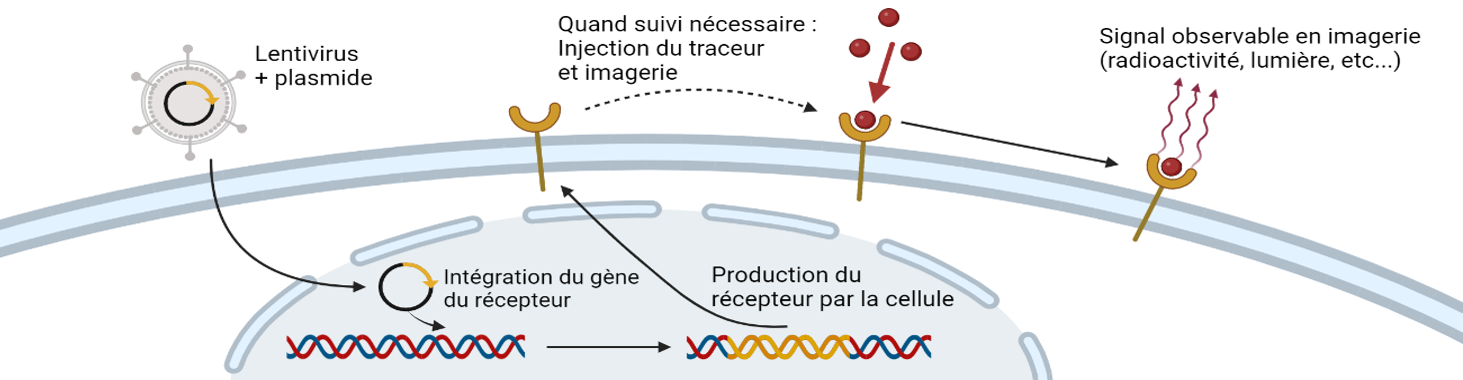
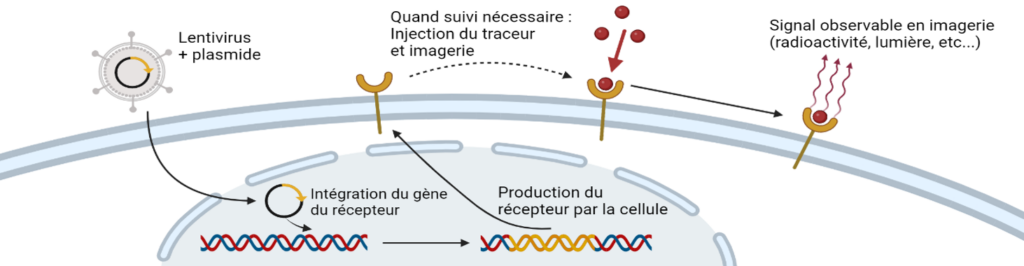
Les thérapies cellulaires sont des thérapies innovantes dans plusieurs pathologies incluant les cancers, les maladies cardiaques et les maladies auto-immunes. La thérapie cellulaire consiste soit à produire des cellules issues d’un donneur sain dans un laboratoire soit à prélever des cellules chez un patient, puis éventuellement à les modifier afin de leur attribuer une fonction précise, pour les réimplanter au patient. Ces thérapies montrent souvent une forte efficacité chez certains patients mais sont parfois accompagnées d’effets indésirables qui peuvent être graves. C’est dans ce contexte que nos projets de recherches visent à donner à ces cellules thérapeutiques des capacités imageantes afin de pouvoir les suivre en temps réel une fois réinjectées chez le patients. Pour cela nous proposons de modifier les cellules afin qu’elles expriment à leur surface des protéines capables de piéger des molécules radioactives pour l’imagerie nucléaire. Ainsi, nous pourrons suivre l’accumulation des cellules au niveau des tumeurs pour évaluer leur efficacité et, dans le même temps, suivre l’accumulation des cellules dans d’autres organes pour évaluer de potentiels effets secondaires. Dans ce contexte nous travaillons en collaboration avec le Dr Alvaro BAEZA GARCIA (INSERM U1231, équipe HSP-pathies, Dr Carmen Garrido).
FIBROSE PULMONAIRE IDIOPATHIQUE
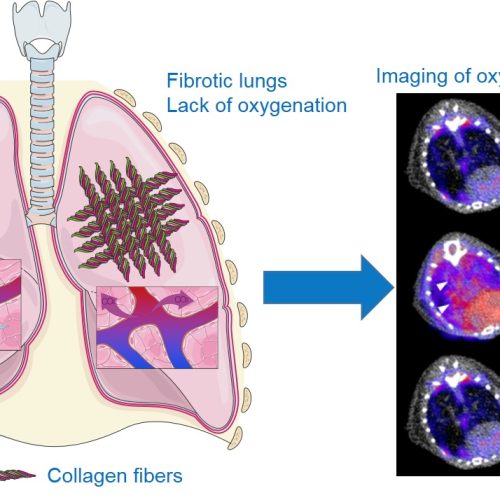
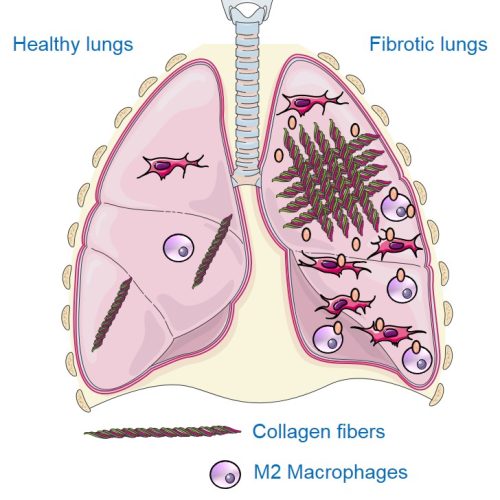
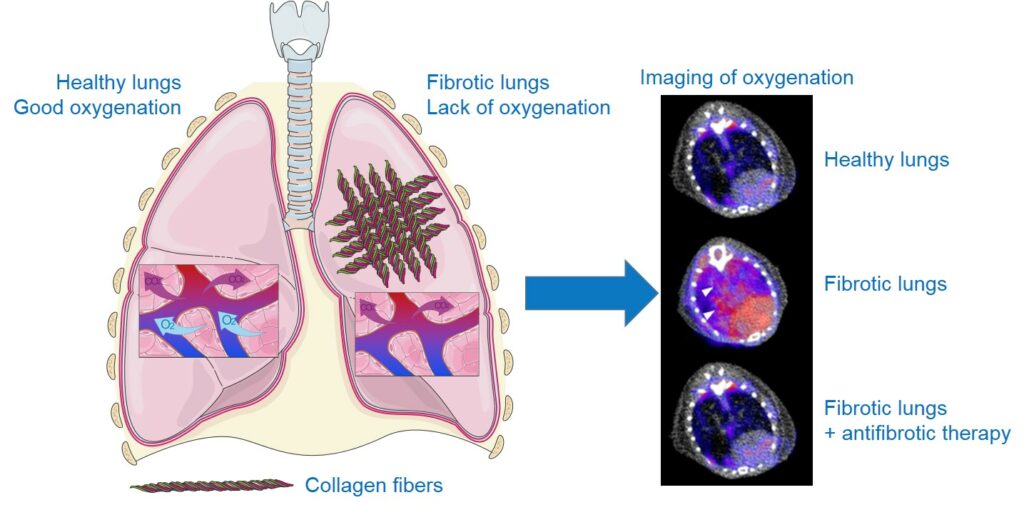
La fibrose pulmonaire idiopathique (FPI) est une maladie rare, irréversible de causes inconnues. Il s’agit d’une maladie chronique caractérisée par une cicatrisation progressive des poumons conduisant à une accumulation de cellules produisant du collagène responsable de la rigidification des poumons. Ainsi, le passage de l’oxygène et le rejet du dioxyde de carbone n’est plus assuré et les patients souffrent principalement de difficultés respiratoires importantes comme un essoufflement progressif, à l’effort puis au repos, une toux sèche chronique ainsi qu’une grande fatigue. La FPI débute généralement après 50 ans et a un pronostic assez sombre avec une médiane de survie d’environ 5 ans après diagnostic. La France compterait un minimum de 12 000 personnes touchées et un minimum de 4400 nouveaux cas chaque année. Les traitements restent très limités avec 2 composés, la pirfenidone et le nintedanib, qui ont montré leur efficacité pour réduire la progression de la maladie sans la stopper complétement. Les difficultés de diagnostic et le manque d’outils pour le suivi de la progression de la maladie et/ou l’efficacité des traitements sont des enjeux cliniques importants. Notre objectif est de trouver des outils d’imagerie nucléaire permettant de faciliter le diagnostic précoce et le suivi des patients afin d’améliorer leur prise en charge et leur survie.
Notre plateforme a obtenu un financement ANR (HYMAGE-IPF) de 240 000 euros sur 3 ans (2020-2023) pour développer, en collaboration avec l’équipe INSERM HSP-pathies dirigé par le Dr Carmen Garrido et le centre de référence des maladies pulmonaires rares du CHU de Dijon dirigé par le Pr Philippe Bonniaud, des traceurs d’imagerie pour la FPI ciblant :
Hypoxie
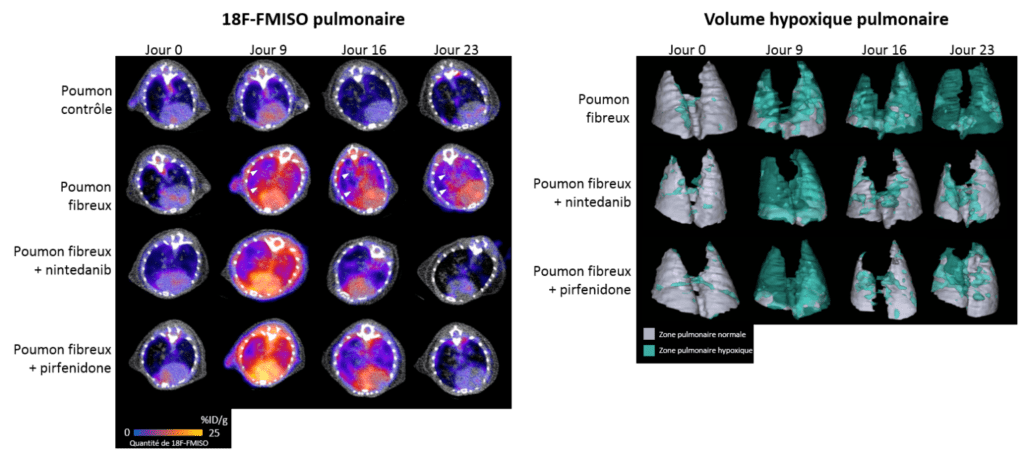
Du fait de la destruction de la structure pulmonaire par l’excès de tissue cicatriciel qui perturbe les échanges gazeux, l’hypoxie (manque d’oxygène) est une caractéristique importante des poumons de patients atteints de FPI. Grâce à l’utilisation d’un radiotraceur spécifique des régions en hypoxie, le 18F-FMISO (molécule radioactive s’accumulant spécifiquement dans les cellules en condition de manque d’oxygène), nous avons pu montrer que les zones d’hypoxie étaient plus importantes dans les poumons en condition de fibrose en corrélation avec la gravité de la maladie. De plus, le taux d’hypoxie pulmonaire mesuré en imagerie avec le 18F-FMISO est un bon marqueur prédictif de la progression de la maladie et de la réponse aux traitements anti-fibrose nintedanib et pirfenidone dans nos modèles précliniques (pour plus de détail voir la publications associée).
Publication associée :
- Tanguy, F. Goirand, A. Bouchard, J. Frenay, M. Moreau, C. Mothes, A. Oudot, A. Helbling, M. Guillemin, P. Bonniaud, A. Cochet, B. Collin, P. S. Bellaye, [18F]FMISO PET/CT imaging of hypoxia as a non-invasive biomarker of disease progression and therapy efficacy in a preclinical model of pulmonary fibrosis: comparison with the [18F]FDG PET/CT approach. Eur J Nucl Med Mol Imaging, (2021).
- Bellaye PS, Beltramo G, Burgy O, Collin B, Cochet A, Bonniaud P. Measurement of hypoxia in the lung in idiopathic pulmonary fibrosis: a matter of control. Eur Respir J. 2022 Jan 27:2102711. doi: 10.1183/13993003.02711-2021.
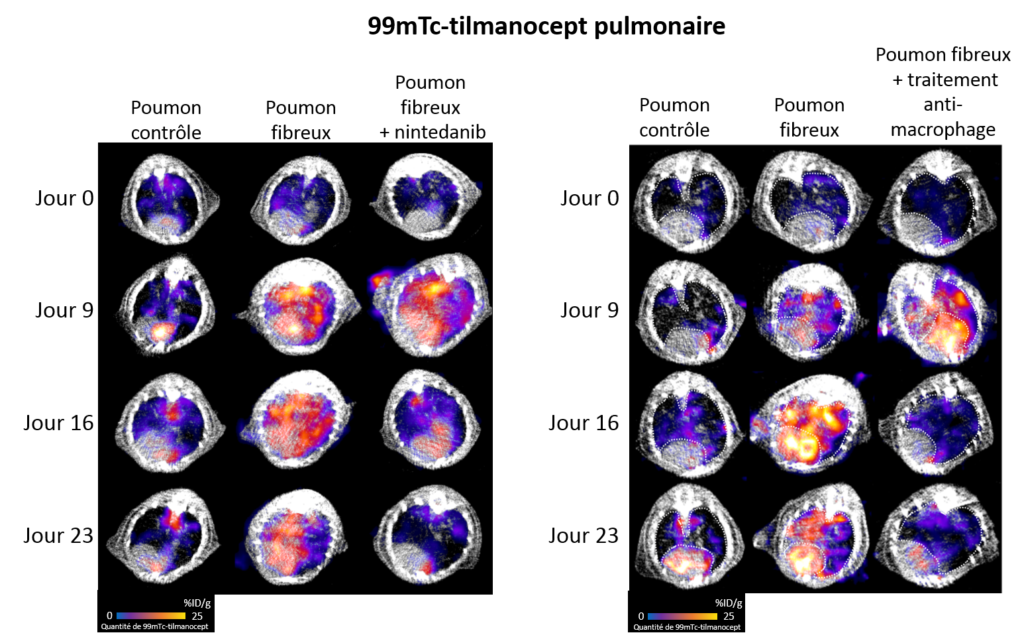
Macrophages
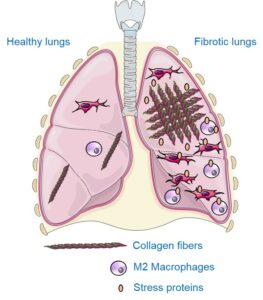
Les macrophages sont des cellules immunitaires circulantes et/ou résidentes dans divers organes notamment les poumons où ils assurent une partie des défenses contre les infections. Dans un contexte de fibrose ces macrophage prennent un phénotype particulier, dit macrophage M2, et secrètent des facteurs de croissance, notamment du TGF-β, qui favorisent la production de tissu cicatriciel dont le collagène. Grâce à l’utilisation d’un radiotraceur spécifique des macrophage M2, le 99mTc-tilmanocept (molécule radioactive se fixant spécifiquement sur les macrophages M2), nous avons pu montrer que les macrophage M2 étaient plus présent dans les poumons en condition de fibrose. De plus, le taux de macrophages M2 pulmonaires mesuré en imagerie avec le 99mTc-tilmanocept permet de suivre précisément la progression de la maladie et la réponse au traitement anti-fibrose nintedanib. Enfin, l’inhibition de ces macrophages agressifs pro-fibrose permet de réduire la progression de la fibrose pulmonaire dans nos modèles précliniques.
Publication associée :
Protéines de choc thermique
Les protéines de choc thermique (ou protéines de stress, HSP) sont des protéines surexprimées en condition de stress pour assurer la survie des cellules. Dans certaines conditions, notamment la fibrose pulmonaire, ces protéines favorisent la progression des maladies. Notre équipe a déjà montré que les HSP sont impliquées dans la surproduction de tissu cicatriciel en condition de fibrose et que leur inhibition est une stratégie prometteuse pour lutter contre cette maladie. Ainsi ce sont des cibles intéressantes pour développer des agents d’imagerie afin de visualiser la progression de la fibrose et la réponse aux traitements. Notre équipe se concentre sur les protéines HSP90 et Gp96 qui sont surexprimées et/ou secrétées en forte quantité chez les patients atteints de FPI et dans les modèles précliniques. Des sondes radioactives spécifiques pour l’imagerie d’HSP90 et Gp96 dans la fibrose sont ainsi en cours de développement chez IMATHERA.
Publication associée:
- J Tanguy , PM Boutanquoi, O Burgy, L Dondaine, G Beltramo, B Uyanik, C Garrido, P Bonniaud, PS Bellaye, F Goirand. HSPB5 Inhibition by NCI-41356 Reduces Experimental Lung Fibrosis by Blocking TGF-β1 Signaling. Pharmaceuticals (Basel). 2023.
- P. S. Bellaye, O. Burgy, P. Bonniaud, M. Kolb, HSP47: a potential target for fibrotic diseases and implications for therapy. Expert Opin Ther Targets 25, 49-62 (2021).
CARDIOLOGIE
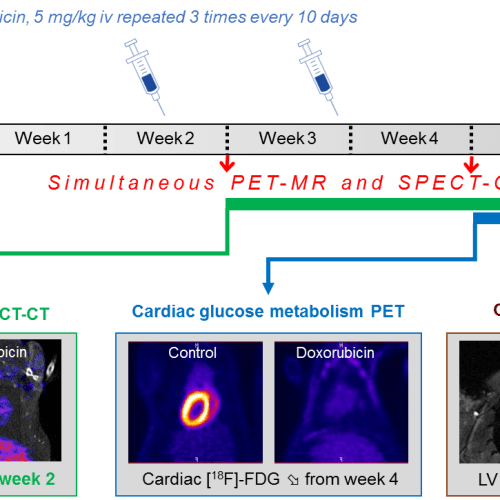
Détection précoce des effets cardiaques des anticancéreux
Au cours des 20 dernières années, le pronostic des patients atteints de cancer n’a cessé de s’améliorer. Cependant, les potentielles complications à long terme de certains traitements, notamment au niveau cardiaque, sont aujourd’hui une préoccupation majeure.
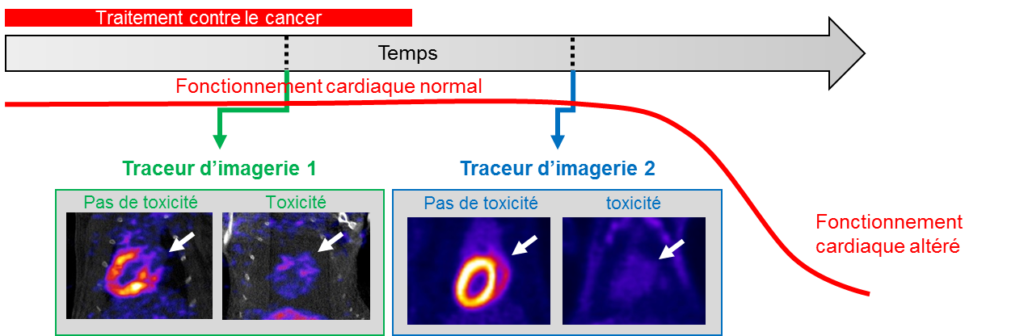
En effet, les complications cardiaques des traitements anticancéreux, bien que rares, sont aujourd’hui prises en charge tardivement lorsque le muscle cardiaque devient moins efficace. L’objectif des travaux menés au laboratoire est de développer des traceurs d’imagerie (molécules injectées aux patients puis détectées par imagerie non invasive) permettant de détecter un impact cardiaque des traitements avant que celui-ci n’affecte la pompe cardiaque.
Publications associées:
MÉTHODOLOGIE EN IMAGERIE PRÉCLINIQUE
La physique médicale et l’instrumentation tiennent une place importante au sein de notre programme de recherche. Ce versant de notre activité est organisé en trois principaux axes.
Instrumentation
- Développement de systèmes innovants d’imagerie en collaboration avec nos partenaires académiques et industriels. Au cours d’IMAPPI, nous avons engagé des collaborations auprès de Bioscan, Trifoil Imaging, et MR Solutions Ltd.
- Etalonnage et réglage fin des imageurs, afin d’obtenir des images morphologiques de haute résolution (CT, IRM) recalées avec des données fonctionnelles quantitatives (SPECT, TEP).
- Réduction des interférences entre les systèmes TEP et IRM.
- Evaluation de performance des imageurs à partir de standards internationaux.
- Conception de protocoles d’assurance de qualité.
- Veille technologique afin de maintenir un haut niveau de performance et d’adaptabilité aux projets scientifiques.
Imagerie du vivant
- Conception de procédures d’imagerie morphologique, quantitative, et fonctionnelle pour répondre aux besoins des équipes de recherche fondamentale ou appliquée.
- Participation à la validation in vivo de l’usage de sondes moléculaires et de nano matériaux, compatibles en particulier avec la TEP/IRM.
Dosimétrie des rayonnements ionisants
- Evaluation de la dose absorbée résultante des examens nucléaires ou radiologiques.
- Optimisation des méthodes d’analyse des données quantitatives.
- Mise en œuvre de la dosimétrie personnalisée des radiothérapies internes vectorisées.
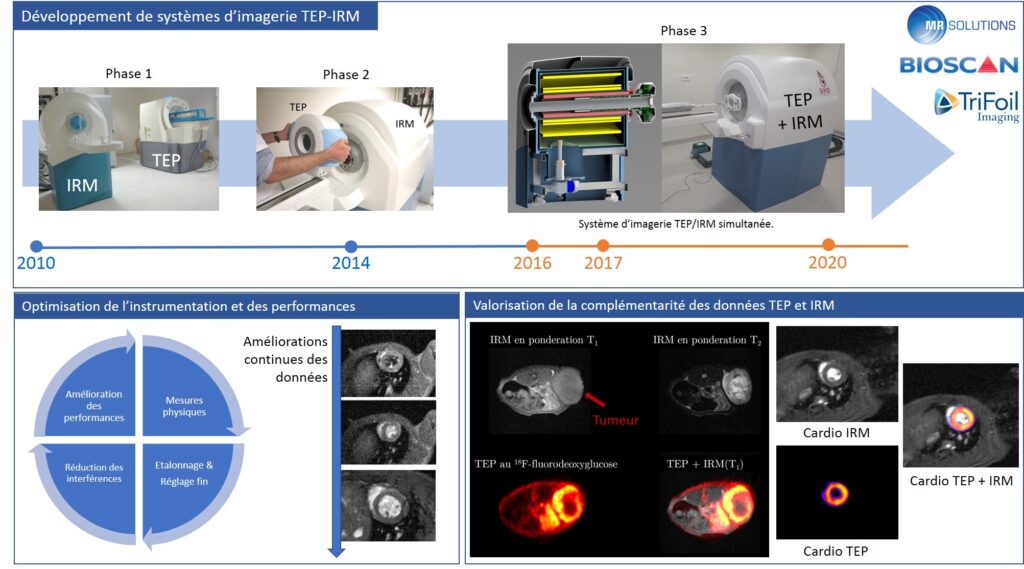
Depuis 2012, la plateforme d’imagerie préclinique accueille le programme Equipex des « investissements d’avenir » IMAPPI (Integrated Magnetic resonance And Positron emission tomography in Preclinical Imaging) financé par l’agence nationale pour la recherche (ANR) à hauteur de 7,3 millons €. Au cours des trois phases de développement du projet IMAPPI, un prototype préclinique d’imagerie TEP/IRM dans lequel la TEP est intégrée au centre de l’aimant d’IRM a été conçu, assemblé, et validé. Ce système, dont les performances ont été publiées en 2021, a depuis été commercialisé et est implanté dans plusieurs équipes de recherche à travers le monde.
A partir de 2021, le projet IMAPPI aborde une nouvelle phase de recherche devant permettre de tirer profit de la haute complémentarité des données de TEP et d’IRM. Nos projets actuels se focalisent entre autres sur les points suivants :
- l’amélioration de l’imagerie cardiaque notamment pour la détection précoce des effets cardiotoxiques des chimiothérapies anticancéreuses et l’imagerie des cardiopathies ischémiques.
- l’imagerie du micro-environnement tumoral et de biomarqueurs d’intérêt en immunothérapie, en particulier la microcirculation et l’oxygénation tissulaire.
- l’intégration des radiomics et de l’intelligence artificielle dans les projets.
Publications associées :
- Courteau, A., J. McGrath, P. M. Walker, B. Presles, R. Garipov, A. Cochet, F. Brunotte, and J. M. Vrigneaud. A Practical Quality Assurance Procedure for Data Acquisitions in Preclinical Simultaneous Pet/Mr Systems. Mol Imaging Biol 25 2023, 450-63
- Courteau A, McGrath J, Walker PM, Pegg R, Martin G, Garipov R, Doughty P, Cochet A, Brunotte F, Vrigneaud JM. Performance Evaluation and Compatibility Studies of a Compact Preclinical Scanner for Simultaneous PET/MR Imaging at 7 Tesla. 2021. IEEE Trans Med Imaging, 40(1):205-217.
- Vrigneaud J.M., McGrath J., Courteau A., Pegg R., Gomis A.S.-P., Camacho A., Martin G., Schramm N., Brunotte F. Initial performance evaluation of a preclinical PET scanner available as a clip-on assembly in a sequential PET/MRI system. 2018. Phys. Med. Biol. 63, 125007.
- S. Bricq, H. L. Kidane, J. Zavala-Bojorquez, A. Oudot, J. M. Vrigneaud, F. Brunotte, P. M. Walker, A. Cochet, A. Lalande, Automatic deformable PET/MRI registration for preclinical studies based on B-splines and non-linear intensity transformation. Med Biol Eng Comput 56, 1531-1539 (2018).
- Vrigneaud J.M., Walker P., Barbier B., Camacho A., Oudot A., Collin B. Brunotte F. Performance evaluation of the PET component of a sequential APD-based micro-PET/MR imaging system. 2017. Biomed. Phys. Eng. Express 3, 035006.
- Pierre-Marc Jodoin, Fredy Pinheiro, Alexandra Oudot, Alain Lalande. Left-Ventricle Segmentation of SPECT Images of Rats. 2015. IEEE Transactions on Biomedical Engineering, Institute of Electrical and Electronics Engineers, 62(9), pp. 2260–2268.
- Brunotte F., Haas H., Collin B., Oudot A., Bricq S., Lalande A., Tizon X., Vrigneaud J.M., Walker P. Integrated PET/MRI in preclinical studies State of the art. Tijdschrift voor nucleaire geneeskunde, 2013, 35
- Vrigneaud JM, Courteau A, Ranouil J, Morgand L, Raguin O, Walker P, Oudot A, Collin B, Brunotte F. Application of the optically stimulated luminescence (OSL) technique for mouse dosimetry in micro-CT imaging. 2013. Med Phys.;40(12):122102.
AUTRES PROJETS ET PARTENAIRES
IMATHERA est également impliquée dans de nombreux autres projets en collaboration avec d’autres équipes de recherche locales ou nationales.
Les projets principaux sont :
Développement d’un agent d’imagerie ciblant les lymphocytes T CD8+ (cytotoxiques) pour visualiser la réponse immunitaire anti-tumorale : projet BIOCAIR. Ce projet et financé par le FEDER.

Imagerie de la protéine PDL1 (cible d’immunothérapie) dans le cancer du colon.
Développement d’agents théranostiques combinant le potentiel de l’imagerie de fluorescence, l’imagerie nucléaire et la thérapie via la thérapie photodynamique (PDT). Ce projet est financé par la SATT-SAYENS.
Nos principaux partenaires :

AUTRES PUBLICATIONS
- Aleksandra Georgievski, Pierre-Simon Bellaye, Benjamin Tournier, Hélène Choubley, Jean-Paul Pais de Barros, Michaële Herbst, Arnaud Béduneau, Patrick Callier, Bertrand Collin, Frédérique Végran, Paola Ballerini, Carmen Garrido, Ronan Quéré. Valrubicin-loaded immunoliposomes for specific vesicle-mediated cell death in the treatment of hematological cancers. Cell Death Dis 2024.
- Kévin Guillen, Pierre-Olivier Comby, Alexandra Oudot, Anne-Virginie Salsac, Nicolas Falvo, Thierry Virely, Olivia Poupardin, Mélanie Guillemin, Olivier Chevallier, Romaric Loffroy. Iodixanol as a New Contrast Agent for Cyanoacrylate Embolization: A Preliminary In Vivo Swine Study. Biomedicines 2023.
- Vivian Lioret, Pierre-Simon Bellaye, Yann Bernhard, Mathieu Moreau, Mélanie Guillemin, Camille Drouet, Bertrand Collin, Richard Decréau. Cherenkov Radiation induced photodynamic therapy – repurposing older photosensitizers, and radionuclides. Photodiagnosis Photodyn Ther 2023.
- Marques, C., M. J. Hajipour, C. Marets, A. Oudot, R. Safavi-Sohi, M. Guillemin, G. Borchard, et al. Identification of the Proteins Determining the Blood Circulation Time of Nanoparticles. ACS Nano 17 2023, 12458-70.
- Nazaryan, S., A. Bruguière, N. Hovhannisyan, T. Miyamoto, A. M. M. Dias, P. S. Bellaye, B. Collin, L. Briand, and C. Mitaine-Offer. Oleanolic Acid Glycosides from Scabiosa Caucasica and Scabiosa Ochroleuca : Structural Analysis and Cytotoxicity. Molecules 28 2023.
- Vizier R, Garnier AR, Dias A, Moreau M, Claron M, Collin B, Denat F, Bellaye PS*, Goncalves V*. SPECT Imaging of Lysyl Oxidase-like 2 in a Model of Idiopathic Pulmonary Fibrosis. Mol Pharm 2023, 20:3613-22.
- Julie Tanguy, Pierre-Marie Boutanquoi, Olivier Burgy, Lucile Dondaine, Guillaume Beltramo, Burhan Uyanik, Carmen Garrido, Philippe Bonniaud, Pierre-Simon Bellaye and Françoise Goirand, HSPB5 Inhibition by NCI-41356 Reduces Experimental Lung Fibrosis by Blocking TGF-β1 Signaling. Pharmaceuticals 2023, 16, 177.
- Jame Frenay, Pierre-Simon Bellaye, Alexandra Oudot, Alex Helbling, Camille Petitot, Christophe Ferrand, Bertrand Collin, Alexandre M. M.Dias, IL-1RAP, a Key Therapeutic Target in Cancer, Int. J. Mol. Sci. 2022, 23(23), 14918.
- Dias AMM, Courteau A, Bellaye PS, Kohli E, Oudot A, Doulain PE, Petitot C, Walker PM, Decréau R, Collin B. Superparamagnetic Iron Oxide Nanoparticles for Immunotherapy of Cancers through Macrophages and Magnetic Hyperthermia. Pharmaceutics. 2022 Nov 5;14(11):2388.
- Baurand PE, Balland J, Reynas C, Ramseyer M, Vivier D, Bellaye PS, Collin B, Paul C, Denat F, Asgarov K, Pallandre JR, Ringenbach L. Development of Anti-LRRC15 Small Fragments for Imaging Purposes Using a Phage-Display ScFv Approach. Int J Mol Sci. 2022 Oct 21;23(20):12677.
- Pertuit D, Mitaine-Offer AC, Miyamoto T, Tanaka C, Delaude C, Bellaye PS, Collin B, Lacaille-Dubois MA. Oleanane-type glycosides isolated from the trunk barks of the Central African tree Millettia laurentii. Fitoterapia. 2022 Jun;159:105193.
- Limagne E, Nuttin L, Thibaudin M, Jacquin E, Aucagne R, Bon M, Revy S, Barnestein R, Ballot E, Truntzer C, Derangère V, Fumet JD, Latour C, Rébé C, Bellaye PS, Kaderbhaï CG, Spill A, Collin B, Callanan MB, Lagrange A, Favier L, Coudert B, Arnould L, Ladoire S, Routy B, Joubert P, Ghiringhelli F. MEK inhibition overcomes chemoimmunotherapy resistance by inducing CXCL10 in cancer cells. Cancer Cell. 2022 Jan 17:S1535-6108(21)00662-0. doi: 10.1016/j.ccell.2021.12.009.
- Nguyen DH, Mitaine-Offer AC, Miyamoto T, Tanaka C, Bellaye PS, Collin B, Chambin O, Lacaille-Dubois MA. Steroidal glycosides from the Vietnamese cultivar Cordyline fruticosa “Fairchild red”. Phytochemistry. 2021 Dec;192:112966.
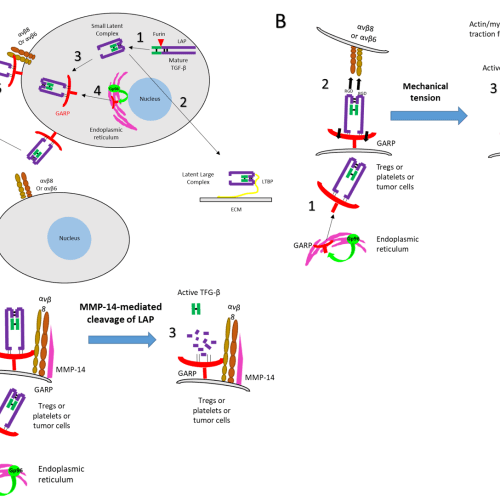
- Bouchard A, Collin B, Garrido C, Bellaye PS, Kohli E. GARP: A Key Target to Evaluate Tumor Immunosuppressive Microenvironment. Biology (Basel). 2021 Aug 27;10(9):836
- E. Renard, M. Moreau, P. S. Bellaye, M. Guillemin, B. Collin, A. Prignon, F. Denat, V. Goncalves, Positron Emission Tomography Imaging of Neurotensin Receptor-Positive Tumors with 68Ga-Labeled Antagonists: The Chelate Makes the Difference Again. J Med Chem 64, 8564-8578 (2021).
- R. Mshaik, J. Simonet, A. Georgievski, L. Jamal, S. Bechoua, P. Ballerini, P. S. Bellaye, Z. Mlamla, J. P. Pais de Barros, A. Geissler, P. J. Francin, F. Girodon, C. Garrido, R. Quéré, HSP90 inhibitor NVP-BEP800 affects stability of SRC kinases and growth of T-cell and B-cell acute lymphoblastic leukemias. Blood Cancer J 11, 61 (2021).
- Marcion, F. Hermetet, F. Neiers, B. Uyanik, L. Dondaine, A. M. M. Dias, L. Da Costa, M. Moreau, P. S. Bellaye, B. Collin, J. Gobbo, L. Briand, R. Seigneuric, O. Kitten, M. Cinier, C. Garrido, Nanofitins targeting heat shock protein 110: An innovative immunotherapeutic modality in cancer. Int J Cancer 148, 3019-3031 (2021).
- Lescure, M. Privat, J. Pliquett, A. Massot, O. Baffroy, B. Busser, P. S. Bellaye, B. Collin, F. Denat, A. Bettaïeb, L. Sancey, C. Paul, C. Goze, E. Bodio, Near-infrared emitting fluorescent homobimetallic gold(I) complexes displaying promising in vitro and in vivo therapeutic properties. Eur J Med Chem 220, 113483 (2021).
- V. Lioret, P. S. Bellaye, C. Arnould, B. Collin, R. A. Decréau, Dual Cherenkov Radiation-Induced Near-Infrared Luminescence Imaging and Photodynamic Therapy toward Tumor Resection. J Med Chem 63, 9446-9456 (2020).
- Hadi, C. Ramseyer, T. Gautier, P. S. Bellaye, T. Lopez, A. Schmitt, S. Foley, S. Yesylevskyy, T. Minervini, R. Douhard, L. Dondaine, L. Proukhnitzky, S. Messaoudi, M. Wendremaire, M. Moreau, F. Neiers, B. Collin, F. Denat, L. Lagrost, C. Garrido, F. Lirussi, Lipoproteins LDL versus HDL as nanocarriers to target either cancer cells or macrophages. JCI Insight 5, (2020).
- O. Florès, J. Pliquett, L. Abad Galan, R. Lescure, F. Denat, O. Maury, A. Pallier, P. S. Bellaye, B. Collin, S. Même, C. S. Bonnet, E. Bodio, C. Goze, Aza-BODIPY Platform: Toward an Efficient Water-Soluble Bimodal Imaging Probe for MRI and Near-Infrared Fluorescence. Inorg Chem 59, 1306-1314 (2020).
- Thomas, J. Boudon, L. Maurizi, M. Moreau, P. Walker, I. Severin, A. Oudot, C. Goze, S. Poty, J. M. Vrigneaud, F. Demoisson, F. Denat, F. Brunotte, N. Millot, Innovative Magnetic Nanoparticles for PET/MRI Bimodal Imaging. ACS Omega 4, 2637-2648 (2019).
- J. Pliquett, A. Dubois, C. Racoeur, N. Mabrouk, S. Amor, R. Lescure, A. Bettaïeb, B. Collin, C. Bernhard, F. Denat, P. S. Bellaye, C. Paul, E. Bodio, C. Goze, A Promising Family of Fluorescent Water-Soluble aza-BODIPY Dyes for in Vivo Molecular Imaging. Bioconjug Chem 30, 1061-1066 (2019).
- D. H. Nguyen, A. C. Mitaine-Offer, S. Maroso, A. M. Papini, T. Paululat, P. S. Bellaye, B. Collin, O. Chambin, M. A. Lacaille-Dubois, Cytotoxic glycosides from the roots of Weigela x \”Bristol Ruby\”. Fitoterapia 137, 104242 (2019).
- A. Loiseau, J. Boudon, A. Oudot, M. Moreau, R. Boidot, R. Chassagnon, N. M. Saïd, S. Roux, C. Mirjolet, N. Millot, Titanate Nanotubes Engineered with Gold Nanoparticles and Docetaxel to Enhance Radiotherapy on Xenografted Prostate Tumors. Cancers (Basel) 11, (2019).
- G. Leterme, C. Guigou, A. Oudot, B. Collin, J. Boudon, N. Millot, A. Geissler, K. Belharet, A. Bozorg Grayeli, Superparamagnetic Nanoparticle Delivery to the Cochlea Through Round Window by External Magnetic Field: Feasibility and Toxicity. Surg Innov 26, 646-655 (2019).
- C. Canovas, M. Moreau, J. M. Vrigneaud, P. S. Bellaye, B. Collin, F. Denat, V. Goncalves, Modular Assembly of Multimodal Imaging Agents through an Inverse Electron Demand Diels-Alder Reaction. Bioconjug Chem 30, 888-897 (2019).
- A. Bernard, S. Chevrier, F. Beltjens, M. Dosset, E. Viltard, A. Lagrange, V. Derangère, A. Oudot, F. Ghiringhelli, B. Collin, L. Apetoh, O. Feron, S. Chen, L. Arnould, F. Végran, R. Boidot, Cleaved Caspase-3 Transcriptionally Regulates Angiogenesis-Promoting Chemotherapy Resistance. Cancer Res 79, 5958-5970 (2019).
- V. L. Tran, V. Thakare, M. Natuzzi, M. Moreau, A. Oudot, J. M. Vrigneaud, A. Courteau, C. Louis, S. Roux, F. Boschetti, F. Denat, O. Tillement, F. Lux, Functionalization of Gadolinium Chelates Silica Nanoparticle through Silane Chemistry for Simultaneous MRI/ 64Cu PET Imaging. Contrast Media Mol Imaging 2018, 7938267 (2018).
- E. Desvaux, A. Courteau, P. S. Bellaye, M. Guillemin, C. Drouet, P. Walker, B. Collin, R. A. Decréau, Cherenkov luminescence imaging is a fast and relevant preclinical tool to assess tumour hypoxia in vivo. EJNMMI Res 8, 111 (2018).
- C. Canovas, M. Moreau, C. Bernhard, A. Oudot, M. Guillemin, F. Denat, V. Goncalves, Site-Specific Dual Labeling of Proteins on Cysteine Residues with Chlorotetrazines. Angew Chem Int Ed Engl 57, 10646-10650 (2018).
- C. Canovas, P. S. Bellaye, M. Moreau, A. Romieu, F. Denat, V. Goncalves, Site-specific near-infrared fluorescent labelling of proteins on cysteine residues with meso-chloro-substituted heptamethine cyanine dyes. Org Biomol Chem 16, 8831-8836 (2018).
- P. S. Bellaye, A. Oudot, J. M. Vrigneaud, O. Raguin, F. Bichat, A. Vaslin, H. Maby-El Hajjami, C. Zanna, G. Vuagniaux, P. Fumoleau, F. Denat, F. Brunotte, B. Collin, Nuclear Imaging Study of the Pharmacodynamic Effects of Debio 1143, an Antagonist of Multiple Inhibitor of Apoptosis Proteins (IAPs), in a Triple-Negative Breast Cancer Model. Contrast Media Mol Imaging 2018, 8494031 (2018).
- P. S. Bellaye, M. Moreau, O. Raguin, A. Oudot, C. Bernhard, J. M. Vrigneaud, L. Dumont, D. Vandroux, F. Denat, A. Cochet, F. Brunotte, B. Collin, Radiolabeled F(ab”) <sub>2</sub>-cetuximab for theranostic purposes in colorectal and skin tumor-bearing mice models. Clin Transl Oncol 20, 1557-1570 (2018).
- M. Moreau, S. Poty, J. M. Vrigneaud, P. Walker, M. Guillemin, O. Raguin, A. Oudot, C. Bernhard, C. Goze, F. Boschetti, B. Collin, F. Brunotte, F. Denat, MANOTA: a promising bifunctional chelating agent for copper-64 immunoPET. Dalton Trans 46, 14659-14668 (2017).
- C. Mirjolet, J. Boudon, A. Loiseau, S. Chevrier, R. Boidot, A. Oudot, B. Collin, E. Martin, P. A. Joy, N. Millot, G. Créhange, Docetaxel-titanate nanotubes enhance radiosensitivity in an androgen-independent prostate cancer model. Int J Nanomedicine 12, 6357-6364 (2017).
- Y. Bernhard, B. Collin, R. A. Decréau, Redshifted Cherenkov Radiation for in vivo Imaging: Coupling Cherenkov Radiation Energy Transfer to multiple Förster Resonance Energy Transfers. Sci Rep 7, 45063 (2017).
- N. Maindron, M. Ipuy, C. Bernhard, D. Lhenry, M. Moreau, S. Carme, A. Oudot, B. Collin, J. M. Vrigneaud, P. Provent, F. Brunotte, F. Denat, C. Goze, Near-Infrared-Emitting BODIPY-trisDOTA(111) In as a Monomolecular Multifunctional Imaging Probe: From Synthesis to In Vivo Investigations. Chemistry 22, 12670-12674 (2016).
- Laurent, C. Bernhard, S. Dufort, G. Jiménez Sánchez, R. Bazzi, F. Boschetti, M. Moreau, T. H. Vu, B. Collin, A. Oudot, N. Herath, H. Requardt, S. Laurent, L. Vander Elst, R. Muller, M. Dutreix, M. Meyer, F. Brunotte, P. Perriat, F. Lux, O. Tillement, G. Le Duc, F. Denat, S. Roux, Minor changes in the macrocyclic ligands but major consequences on the efficiency of gold nanoparticles designed for radiosensitization. Nanoscale 8, 12054-12065 (2016).
- D. Lhenry, M. Larrouy, C. Bernhard, V. Goncalves, O. Raguin, P. Provent, M. Moreau, B. Collin, A. Oudot, J. M. Vrigneaud, F. Brunotte, C. Goze, F. Denat, BODIPY: A Highly Versatile Platform for the Design of Bimodal Imaging Probes. Chemistry 21, 13091-13099 (2015).
- M. Jodoin, F. Pinheiro, A. Oudot, A. Lalande, Left-Ventricle Segmentation of SPECT Images of Rats. IEEE Trans Biomed Eng 62, 2260-2268 (2015).
- Duheron, M. Moreau, B. Collin, W. Sali, C. Bernhard, C. Goze, T. Gautier, J. P. Pais de Barros, V. Deckert, F. Brunotte, L. Lagrost, F. Denat, Dual labeling of lipopolysaccharides for SPECT-CT imaging and fluorescence microscopy. ACS Chem Biol 9, 656-662 (2014).
- De Taddéo, B. Collin, H. Hardy, B. Guichard, P. Trouilloud, O. Trost, [Can one harvest a long bone stick in the radial forearm flap? Original radioanatomical and NanoSPECT-CT Bioscan microvascular study]. Ann Chir Plast Esthet 59, 170-176 (2014).
- Y. Bernhard, B. Collin, R. A. Decréau, Inter/intramolecular Cherenkov radiation energy transfer (CRET) from a fluorophore with a built-in radionuclide. Chem Commun (Camb) 50, 6711-6713 (2014).
- J. M. Vrigneaud, A. Courteau, J. Ranouil, L. Morgand, O. Raguin, P. Walker, A. Oudot, B. Collin, F. Brunotte, Application of the optically stimulated luminescence (OSL) technique for mouse dosimetry in micro-CT imaging. Med Phys 40, 122102 (2013).
- F. Végran, R. Mary, A. Gibeaud, C. Mirjolet, B. Collin, A. Oudot, C. Charon-Barra, L. Arnould, S. Lizard-Nacol, R. Boidot, Survivin-3B potentiates immune escape in cancer but also inhibits the toxicity of cancer chemotherapy. Cancer Res 73, 5391-5401 (2013).
- Moreau, O. Raguin, J. M. Vrigneaud, B. Collin, C. Bernhard, X. Tizon, F. Boschetti, O. Duchamp, F. Brunotte, F. Denat, DOTAGA-trastuzumab. A new antibody conjugate targeting HER2/Neu antigen for diagnostic purposes. Bioconjug Chem 23, 1181-1188 (2012).
- * Crédit photo mise en avant: A. Chezières
Les actualités de la plateforme
Autres publications
- Aleksandra Georgievski, Pierre-Simon Bellaye, Benjamin Tournier, Hélène Choubley, Jean-Paul Pais de Barros, Michaële Herbst, Arnaud Béduneau, Patrick Callier, Bertrand Collin, Frédérique Végran, Paola Ballerini, Carmen Garrido, Ronan Quéré. Valrubicin-loaded immunoliposomes for specific vesicle-mediated cell death in the treatment of hematological cancers. Cell Death Dis 2024.
- Kévin Guillen, Pierre-Olivier Comby, Alexandra Oudot, Anne-Virginie Salsac, Nicolas Falvo, Thierry Virely, Olivia Poupardin, Mélanie Guillemin, Olivier Chevallier, Romaric Loffroy. Iodixanol as a New Contrast Agent for Cyanoacrylate Embolization: A Preliminary In Vivo Swine Study. Biomedicines 2023.
- Vivian Lioret, Pierre-Simon Bellaye, Yann Bernhard, Mathieu Moreau, Mélanie Guillemin, Camille Drouet, Bertrand Collin, Richard Decréau. Cherenkov Radiation induced photodynamic therapy – repurposing older photosensitizers, and radionuclides. Photodiagnosis Photodyn Ther 2023.
- Marques, C., M. J. Hajipour, C. Marets, A. Oudot, R. Safavi-Sohi, M. Guillemin, G. Borchard, et al. Identification of the Proteins Determining the Blood Circulation Time of Nanoparticles. ACS Nano 17 2023, 12458-70.
- Nazaryan, S., A. Bruguière, N. Hovhannisyan, T. Miyamoto, A. M. M. Dias, P. S. Bellaye, B. Collin, L. Briand, and C. Mitaine-Offer. Oleanolic Acid Glycosides from Scabiosa Caucasica and Scabiosa Ochroleuca : Structural Analysis and Cytotoxicity. Molecules 28 2023.
- Vizier R, Garnier AR, Dias A, Moreau M, Claron M, Collin B, Denat F, Bellaye PS*, Goncalves V*. SPECT Imaging of Lysyl Oxidase-like 2 in a Model of Idiopathic Pulmonary Fibrosis. Mol Pharm 2023, 20:3613-22.
- Julie Tanguy, Pierre-Marie Boutanquoi, Olivier Burgy, Lucile Dondaine, Guillaume Beltramo, Burhan Uyanik, Carmen Garrido, Philippe Bonniaud, Pierre-Simon Bellaye and Françoise Goirand, HSPB5 Inhibition by NCI-41356 Reduces Experimental Lung Fibrosis by Blocking TGF-β1 Signaling. Pharmaceuticals 2023, 16, 177.
- Jame Frenay, Pierre-Simon Bellaye, Alexandra Oudot, Alex Helbling, Camille Petitot, Christophe Ferrand, Bertrand Collin, Alexandre M. M.Dias, IL-1RAP, a Key Therapeutic Target in Cancer, Int. J. Mol. Sci. 2022, 23(23), 14918.
- Dias AMM, Courteau A, Bellaye PS, Kohli E, Oudot A, Doulain PE, Petitot C, Walker PM, Decréau R, Collin B. Superparamagnetic Iron Oxide Nanoparticles for Immunotherapy of Cancers through Macrophages and Magnetic Hyperthermia. Pharmaceutics. 2022 Nov 5;14(11):2388.
- Baurand PE, Balland J, Reynas C, Ramseyer M, Vivier D, Bellaye PS, Collin B, Paul C, Denat F, Asgarov K, Pallandre JR, Ringenbach L. Development of Anti-LRRC15 Small Fragments for Imaging Purposes Using a Phage-Display ScFv Approach. Int J Mol Sci. 2022 Oct 21;23(20):12677.
- Pertuit D, Mitaine-Offer AC, Miyamoto T, Tanaka C, Delaude C, Bellaye PS, Collin B, Lacaille-Dubois MA. Oleanane-type glycosides isolated from the trunk barks of the Central African tree Millettia laurentii. Fitoterapia. 2022 Jun;159:105193.
- Limagne E, Nuttin L, Thibaudin M, Jacquin E, Aucagne R, Bon M, Revy S, Barnestein R, Ballot E, Truntzer C, Derangère V, Fumet JD, Latour C, Rébé C, Bellaye PS, Kaderbhaï CG, Spill A, Collin B, Callanan MB, Lagrange A, Favier L, Coudert B, Arnould L, Ladoire S, Routy B, Joubert P, Ghiringhelli F. MEK inhibition overcomes chemoimmunotherapy resistance by inducing CXCL10 in cancer cells. Cancer Cell. 2022 Jan 17:S1535-6108(21)00662-0. doi: 10.1016/j.ccell.2021.12.009.
- Nguyen DH, Mitaine-Offer AC, Miyamoto T, Tanaka C, Bellaye PS, Collin B, Chambin O, Lacaille-Dubois MA. Steroidal glycosides from the Vietnamese cultivar Cordyline fruticosa “Fairchild red”. Phytochemistry. 2021 Dec;192:112966.
- Bouchard A, Collin B, Garrido C, Bellaye PS, Kohli E. GARP: A Key Target to Evaluate Tumor Immunosuppressive Microenvironment. Biology (Basel). 2021 Aug 27;10(9):836
- E. Renard, M. Moreau, P. S. Bellaye, M. Guillemin, B. Collin, A. Prignon, F. Denat, V. Goncalves, Positron Emission Tomography Imaging of Neurotensin Receptor-Positive Tumors with 68Ga-Labeled Antagonists: The Chelate Makes the Difference Again. J Med Chem 64, 8564-8578 (2021).
- R. Mshaik, J. Simonet, A. Georgievski, L. Jamal, S. Bechoua, P. Ballerini, P. S. Bellaye, Z. Mlamla, J. P. Pais de Barros, A. Geissler, P. J. Francin, F. Girodon, C. Garrido, R. Quéré, HSP90 inhibitor NVP-BEP800 affects stability of SRC kinases and growth of T-cell and B-cell acute lymphoblastic leukemias. Blood Cancer J 11, 61 (2021).
- Marcion, F. Hermetet, F. Neiers, B. Uyanik, L. Dondaine, A. M. M. Dias, L. Da Costa, M. Moreau, P. S. Bellaye, B. Collin, J. Gobbo, L. Briand, R. Seigneuric, O. Kitten, M. Cinier, C. Garrido, Nanofitins targeting heat shock protein 110: An innovative immunotherapeutic modality in cancer. Int J Cancer 148, 3019-3031 (2021).
- Lescure, M. Privat, J. Pliquett, A. Massot, O. Baffroy, B. Busser, P. S. Bellaye, B. Collin, F. Denat, A. Bettaïeb, L. Sancey, C. Paul, C. Goze, E. Bodio, Near-infrared emitting fluorescent homobimetallic gold(I) complexes displaying promising in vitro and in vivo therapeutic properties. Eur J Med Chem 220, 113483 (2021).
- V. Lioret, P. S. Bellaye, C. Arnould, B. Collin, R. A. Decréau, Dual Cherenkov Radiation-Induced Near-Infrared Luminescence Imaging and Photodynamic Therapy toward Tumor Resection. J Med Chem 63, 9446-9456 (2020).
- Hadi, C. Ramseyer, T. Gautier, P. S. Bellaye, T. Lopez, A. Schmitt, S. Foley, S. Yesylevskyy, T. Minervini, R. Douhard, L. Dondaine, L. Proukhnitzky, S. Messaoudi, M. Wendremaire, M. Moreau, F. Neiers, B. Collin, F. Denat, L. Lagrost, C. Garrido, F. Lirussi, Lipoproteins LDL versus HDL as nanocarriers to target either cancer cells or macrophages. JCI Insight 5, (2020).
- O. Florès, J. Pliquett, L. Abad Galan, R. Lescure, F. Denat, O. Maury, A. Pallier, P. S. Bellaye, B. Collin, S. Même, C. S. Bonnet, E. Bodio, C. Goze, Aza-BODIPY Platform: Toward an Efficient Water-Soluble Bimodal Imaging Probe for MRI and Near-Infrared Fluorescence. Inorg Chem 59, 1306-1314 (2020).
- Thomas, J. Boudon, L. Maurizi, M. Moreau, P. Walker, I. Severin, A. Oudot, C. Goze, S. Poty, J. M. Vrigneaud, F. Demoisson, F. Denat, F. Brunotte, N. Millot, Innovative Magnetic Nanoparticles for PET/MRI Bimodal Imaging. ACS Omega 4, 2637-2648 (2019).
- J. Pliquett, A. Dubois, C. Racoeur, N. Mabrouk, S. Amor, R. Lescure, A. Bettaïeb, B. Collin, C. Bernhard, F. Denat, P. S. Bellaye, C. Paul, E. Bodio, C. Goze, A Promising Family of Fluorescent Water-Soluble aza-BODIPY Dyes for in Vivo Molecular Imaging. Bioconjug Chem 30, 1061-1066 (2019).
- D. H. Nguyen, A. C. Mitaine-Offer, S. Maroso, A. M. Papini, T. Paululat, P. S. Bellaye, B. Collin, O. Chambin, M. A. Lacaille-Dubois, Cytotoxic glycosides from the roots of Weigela x \”Bristol Ruby\”. Fitoterapia 137, 104242 (2019).
- A. Loiseau, J. Boudon, A. Oudot, M. Moreau, R. Boidot, R. Chassagnon, N. M. Saïd, S. Roux, C. Mirjolet, N. Millot, Titanate Nanotubes Engineered with Gold Nanoparticles and Docetaxel to Enhance Radiotherapy on Xenografted Prostate Tumors. Cancers (Basel) 11, (2019).
- G. Leterme, C. Guigou, A. Oudot, B. Collin, J. Boudon, N. Millot, A. Geissler, K. Belharet, A. Bozorg Grayeli, Superparamagnetic Nanoparticle Delivery to the Cochlea Through Round Window by External Magnetic Field: Feasibility and Toxicity. Surg Innov 26, 646-655 (2019).
- C. Canovas, M. Moreau, J. M. Vrigneaud, P. S. Bellaye, B. Collin, F. Denat, V. Goncalves, Modular Assembly of Multimodal Imaging Agents through an Inverse Electron Demand Diels-Alder Reaction. Bioconjug Chem 30, 888-897 (2019).
- A. Bernard, S. Chevrier, F. Beltjens, M. Dosset, E. Viltard, A. Lagrange, V. Derangère, A. Oudot, F. Ghiringhelli, B. Collin, L. Apetoh, O. Feron, S. Chen, L. Arnould, F. Végran, R. Boidot, Cleaved Caspase-3 Transcriptionally Regulates Angiogenesis-Promoting Chemotherapy Resistance. Cancer Res 79, 5958-5970 (2019).
- V. L. Tran, V. Thakare, M. Natuzzi, M. Moreau, A. Oudot, J. M. Vrigneaud, A. Courteau, C. Louis, S. Roux, F. Boschetti, F. Denat, O. Tillement, F. Lux, Functionalization of Gadolinium Chelates Silica Nanoparticle through Silane Chemistry for Simultaneous MRI/ <sup>64</sup>Cu PET Imaging. Contrast Media Mol Imaging 2018, 7938267 (2018).
- E. Desvaux, A. Courteau, P. S. Bellaye, M. Guillemin, C. Drouet, P. Walker, B. Collin, R. A. Decréau, Cherenkov luminescence imaging is a fast and relevant preclinical tool to assess tumour hypoxia in vivo. EJNMMI Res 8, 111 (2018).
- C. Canovas, M. Moreau, C. Bernhard, A. Oudot, M. Guillemin, F. Denat, V. Goncalves, Site-Specific Dual Labeling of Proteins on Cysteine Residues with Chlorotetrazines. Angew Chem Int Ed Engl 57, 10646-10650 (2018).
- C. Canovas, P. S. Bellaye, M. Moreau, A. Romieu, F. Denat, V. Goncalves, Site-specific near-infrared fluorescent labelling of proteins on cysteine residues with meso-chloro-substituted heptamethine cyanine dyes. Org Biomol Chem 16, 8831-8836 (2018).
- P. S. Bellaye, A. Oudot, J. M. Vrigneaud, O. Raguin, F. Bichat, A. Vaslin, H. Maby-El Hajjami, C. Zanna, G. Vuagniaux, P. Fumoleau, F. Denat, F. Brunotte, B. Collin, Nuclear Imaging Study of the Pharmacodynamic Effects of Debio 1143, an Antagonist of Multiple Inhibitor of Apoptosis Proteins (IAPs), in a Triple-Negative Breast Cancer Model. Contrast Media Mol Imaging 2018, 8494031 (2018).
- P. S. Bellaye, M. Moreau, O. Raguin, A. Oudot, C. Bernhard, J. M. Vrigneaud, L. Dumont, D. Vandroux, F. Denat, A. Cochet, F. Brunotte, B. Collin, Radiolabeled F(ab”) <sub>2</sub>-cetuximab for theranostic purposes in colorectal and skin tumor-bearing mice models. Clin Transl Oncol 20, 1557-1570 (2018).
- M. Moreau, S. Poty, J. M. Vrigneaud, P. Walker, M. Guillemin, O. Raguin, A. Oudot, C. Bernhard, C. Goze, F. Boschetti, B. Collin, F. Brunotte, F. Denat, MANOTA: a promising bifunctional chelating agent for copper-64 immunoPET. Dalton Trans 46, 14659-14668 (2017).
- C. Mirjolet, J. Boudon, A. Loiseau, S. Chevrier, R. Boidot, A. Oudot, B. Collin, E. Martin, P. A. Joy, N. Millot, G. Créhange, Docetaxel-titanate nanotubes enhance radiosensitivity in an androgen-independent prostate cancer model. Int J Nanomedicine 12, 6357-6364 (2017).
- Y. Bernhard, B. Collin, R. A. Decréau, Redshifted Cherenkov Radiation for in vivo Imaging: Coupling Cherenkov Radiation Energy Transfer to multiple Förster Resonance Energy Transfers. Sci Rep 7, 45063 (2017).
- N. Maindron, M. Ipuy, C. Bernhard, D. Lhenry, M. Moreau, S. Carme, A. Oudot, B. Collin, J. M. Vrigneaud, P. Provent, F. Brunotte, F. Denat, C. Goze, Near-Infrared-Emitting BODIPY-trisDOTA(111) In as a Monomolecular Multifunctional Imaging Probe: From Synthesis to In Vivo Investigations. Chemistry 22, 12670-12674 (2016).
- Laurent, C. Bernhard, S. Dufort, G. Jiménez Sánchez, R. Bazzi, F. Boschetti, M. Moreau, T. H. Vu, B. Collin, A. Oudot, N. Herath, H. Requardt, S. Laurent, L. Vander Elst, R. Muller, M. Dutreix, M. Meyer, F. Brunotte, P. Perriat, F. Lux, O. Tillement, G. Le Duc, F. Denat, S. Roux, Minor changes in the macrocyclic ligands but major consequences on the efficiency of gold nanoparticles designed for radiosensitization. Nanoscale 8, 12054-12065 (2016).
- D. Lhenry, M. Larrouy, C. Bernhard, V. Goncalves, O. Raguin, P. Provent, M. Moreau, B. Collin, A. Oudot, J. M. Vrigneaud, F. Brunotte, C. Goze, F. Denat, BODIPY: A Highly Versatile Platform for the Design of Bimodal Imaging Probes. Chemistry 21, 13091-13099 (2015).
- M. Jodoin, F. Pinheiro, A. Oudot, A. Lalande, Left-Ventricle Segmentation of SPECT Images of Rats. IEEE Trans Biomed Eng 62, 2260-2268 (2015).
- Duheron, M. Moreau, B. Collin, W. Sali, C. Bernhard, C. Goze, T. Gautier, J. P. Pais de Barros, V. Deckert, F. Brunotte, L. Lagrost, F. Denat, Dual labeling of lipopolysaccharides for SPECT-CT imaging and fluorescence microscopy. ACS Chem Biol 9, 656-662 (2014).
- De Taddéo, B. Collin, H. Hardy, B. Guichard, P. Trouilloud, O. Trost, [Can one harvest a long bone stick in the radial forearm flap? Original radioanatomical and NanoSPECT-CT Bioscan microvascular study]. Ann Chir Plast Esthet 59, 170-176 (2014).
- Y. Bernhard, B. Collin, R. A. Decréau, Inter/intramolecular Cherenkov radiation energy transfer (CRET) from a fluorophore with a built-in radionuclide. Chem Commun (Camb) 50, 6711-6713 (2014).
- J. M. Vrigneaud, A. Courteau, J. Ranouil, L. Morgand, O. Raguin, P. Walker, A. Oudot, B. Collin, F. Brunotte, Application of the optically stimulated luminescence (OSL) technique for mouse dosimetry in micro-CT imaging. Med Phys 40, 122102 (2013).
- F. Végran, R. Mary, A. Gibeaud, C. Mirjolet, B. Collin, A. Oudot, C. Charon-Barra, L. Arnould, S. Lizard-Nacol, R. Boidot, Survivin-3B potentiates immune escape in cancer but also inhibits the toxicity of cancer chemotherapy. Cancer Res 73, 5391-5401 (2013).
- Moreau, O. Raguin, J. M. Vrigneaud, B. Collin, C. Bernhard, X. Tizon, F. Boschetti, O. Duchamp, F. Brunotte, F. Denat, DOTAGA-trastuzumab. A new antibody conjugate targeting HER2/Neu antigen for diagnostic purposes. Bioconjug Chem 23, 1181-1188 (2012).